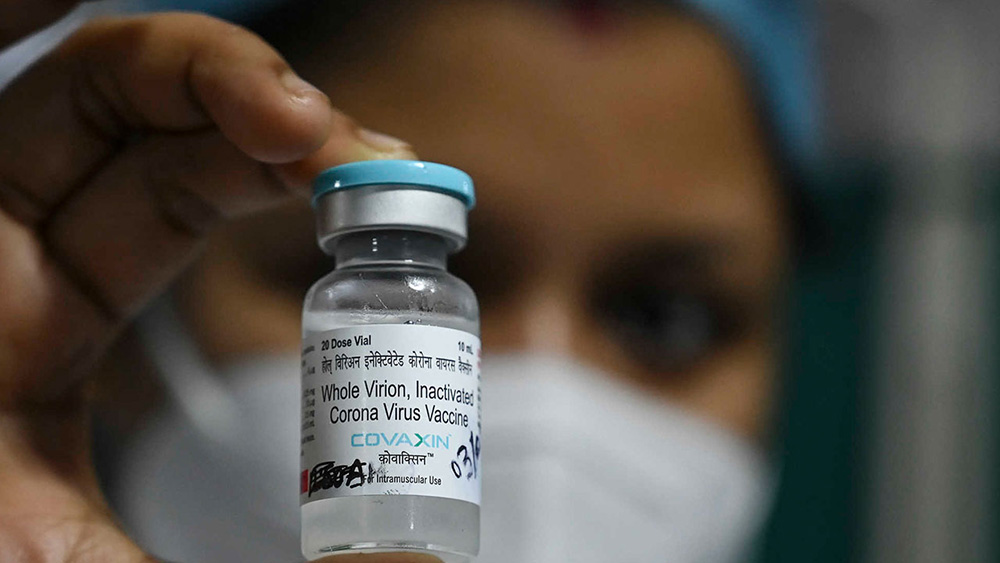
Brasil dio este martes un duro revés no solo a la intención del presidente de este país, Jair Bolsonaro, de comprar 20 millones de dosis de las vacunas indias Covaxin, sino también a las intenciones temporales de aplicarlas en Paraguay.
Y es que en la jornada de ayer llegó al aeropuerto Silvio Pettirossi de la ciudad de Luque un primer cargamento de 100.000 dosis de esta vacuna donadas por el Gobierno de India, como parte de una donación de 200.000 componentes, pero aún no pueden aplicarse porque no hay un permiso oficial de un regulador regional.
Paraguay depende de la Agencia Nacional de Vigilancia Sanitaria (Anvisa) del Brasil y la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) de México para poder usar estas vacunas, ya que ambas son referencias regionales para la autorización sanitaria.
Según CNN Brasil, Anvisa reportó a través del Diario Oficial de la Unión (Gaceta Oficial) que rechazó el pedido de Certificación de Buenas Prácticas para las vacunas Covaxin, el primer paso para tener el permiso de uso de emergencia. La solicitud fue hecha por la empresa brasileña “Precisa-Comercialização de Medicamentos Ltda”, en representación de Bharat Biotech, que fabrica las vacunas en India.
“En la justificación presentada por Anvisa se citó el incumplimiento de tres artículos de la Resolución de la Junta Directiva Colegiada (RDC) 69/2014 de la agencia, que hacen referencia a los documentos que deben presentarse en el proceso, a la especificaciones que deben establecerse para intermediarios e insumos farmacéuticos activos y la validación de los métodos farmacopédicos utilizados por la empresa”, dice la publicación.
Además, dice CNN citando a Anvisa, “se deben adoptar cinco artículos de la Instrucción Normativa (IN) 36/2019 de Anvisa, que tratan de los parámetros críticos del proceso operativo que afectan la calidad del producto, los métodos utilizados para la esterilización y las medidas para evitar el riesgo de nueva contaminación de los productos, de un proceso para asegurar la inactivación completa del organismo vivo, entre otros problemas”.
Añade el texto: “La decisión de la agencia también cita la violación de tres artículos previstos en la EN 35/2019: 108, 154 y 158, que se refieren al monitoreo de la biocarga, sobre el tiempo requerido para filtrar un volumen conocido de la solución a granel y determinar que el filtro no debe afectar al producto”.
Por último, sostiene que “finalmente, también se incluyó en la resolución el incumplimiento del artículo 94 de la EN 47/2019, que establece que ‘todos los métodos analíticos, utilizados en la calificación, validación o limpieza, deben ser validados también con los límites de detección y cuantificación adecuados’”.
Además de la donación de 200.000 dosis recibida por parte del Gobierno de la India, el Ministerio de Salud de Paraguay tramitó la compra de unas 2.000.000 de dosis de esta vacuna que ya fue aplicada a al menos 25 millones de personas en el país asiático.
De momento, la cartera sanitaria paraguaya almacenó las dosis donadas en espera de la aprobación de la Covaxin para iniciar la aplicación de los biológicos en la población.
El embajador de la India concurrente en el país, Dinesh Bhati, dijo que la vacuna está “investigada, desarrollada y producida en la India” y obtuvo un 81 % de eficacia en la fase 3 de las investigaciones.
Hasta la fecha, Paraguay recibió 163.000 dosis de vacunas contra el COVID-19, entre las cuales se encuentran las 4.000 dosis de Sputnik V; las 20.000 dosis de la vacuna CoronaVac donadas por Chile; 3.000 dosis de Sinopharm donadas por Emiratos Árabes, y 36.000 dosis de AstraZeneca que llegaron a través del mecanismo Covax.
Fuente: Medios Digitales